Fmoc-OSu pulver, også kendt som 9-Fluorenylmethoxycarbonyl N-hydroxysuccinimidester, er et reagens, der almindeligvis anvendes inden for peptidsyntese. Det bruges til beskyttelse og aktivering af aminosyrer under fastfase peptidsyntese. Fmoc er en kemisk gruppe, der beskytter en aminosyres aminfunktion, og OSu (N-hydroxysuccinimidester) er en reaktiv gruppe, der letter koblingen af den beskyttede aminosyre til den voksende peptidkæde. Samlet set spiller Fmoc-OSu en afgørende rolle i den trinvise samling af peptider på et fast underlag, hvilket muliggør kontrolleret tilsætning af aminosyrer i den ønskede sekvens.

Hvad er brugen af Fmoc OSu
Fmoc-OSu, også kendt som 9-Fluorenylmethoxycarbonyl N-hydroxysuccinimidester, er almindeligt anvendt inden for peptidsyntese. Det fungerer som et reagens til beskyttelse og aktivering af aminosyrer under fastfase peptidsyntese.
I peptidsyntese anvendes Fmoc-OSu til følgende formål:
1. Beskyttelse af aminogrupper: Fmoc-gruppen beskytter en aminosyres aminfunktion og forhindrer uønskede reaktioner på dette sted under synteseprocessen.
2. Aktivering af aminosyrer: OSu (N-hydroxysuccinimid ester) delen på Fmoc-OSu letter koblingen af beskyttede aminosyrer til voksende peptidkæder. Det er involveret i dannelsen af en amidbinding mellem aminosyrer, afgørende for at forlænge peptidkæden.
Samlet set spiller Fmoc-OSu en kritisk rolle i den kontrollerede samling af peptider på et fast underlag. Det giver mulighed for sekventiel tilføjelse af aminosyrer i en ønsket rækkefølge under fastfase peptidsyntese.
Hvorfor bruges Fmoc i peptidsyntese
Fmoc (9-Fluorenylmethoxycarbonyl) er en almindeligt anvendt beskyttelsesgruppe i peptidsyntese på grund af flere fordelagtige egenskaber, den tilbyder:
1. Ortogonal afbeskyttelse: Fmoc kan fjernes selektivt under milde basisbetingelser (f.eks. med piperidin), hvilket efterlader andre beskyttende grupper som sidekædebeskyttelse intakte. Dette muliggør trinvis afbeskyttelse af individuelle aminosyrer i en syntetisk peptidsekvens.
2. Fastfase-syntesekompatibilitet: Fmoc-kemi er velegnet til fastfase-peptidsyntese, da Fmoc-afbeskyttelsesreaktioner er kompatible med det harpiksbundne peptid. Dette muliggør trinvis tilføjelse af aminosyrer til den voksende peptidkæde.

3. Opløselighed: Peptider syntetiseret ved hjælp af Fmoc-strategien er typisk opløselige i almindelige organiske opløsningsmidler, hvilket gør oprensningstrinene mere håndterbare.
4. Høje koblingsudbytter: Fmoc-baseret peptidsyntese resulterer typisk i høje koblingsudbytter, hvilket fører til effektiv konstruktion af peptidsekvenser med minimal dannelse af uønskede biprodukter.
5. Kommerciel tilgængelighed: Fmoc-beskyttede aminosyrer og relaterede reagenser er let tilgængelige kommercielt, hvilket giver bekvemmelighed og tilgængelighed af nødvendige byggesten til peptidsyntese.
6. Kompatibilitet med fastfasesyntese: Fmoc-baseret fastfase-peptidsyntese er meget udbredt på grund af kompatibiliteten af Fmoc-afbeskyttelsesbetingelser med det harpiksbundne peptid, hvilket muliggør trinvis tilføjelse af aminosyrer til den voksende peptidkæde.

7. Milde reaktionsbetingelser: Fmoc-afbeskyttelsesreaktioner kan udføres under milde betingelser, hvilket reducerer sandsynligheden for uønskede sidereaktioner eller modifikationer af følsomme aminosyresidekæder.
Samlet set gør Fmoc-kemiens alsidighed, selektivitet og kompatibilitet det til et foretrukket valg i peptidsyntese, hvilket giver mulighed for effektiv konstruktion af komplekse peptidsekvenser med præcis kontrol over hvert trin.
Hvilke betingelser kræves for at fjerne Fmoc
Beskyttelsesgruppen 9-fluorenylmethyloxycarbonyl (Fmoc) fjernes almindeligvis under milde basiske forhold under fastfase-peptidsyntese. Standardproceduren for Fmoc-afbeskyttelse involverer anvendelsen af en base, typisk piperidin, i et organisk opløsningsmiddel såsom N,N-dimethylformamid (DMF) eller en blanding af DMF og et co-opløsningsmiddel som dichlormethan.
En almindelig metode til Fmoc-afbeskyttelse involverer behandling med en opløsning af piperidin i DMF. Reaktionen udføres typisk i en kort varighed, ofte nogle få minutter, ved stuetemperatur eller let forhøjede temperaturer. Naturen af den Fmoc-beskyttede aminosyre og de særlige krav til peptidsyntese kan tages i betragtning, mens temperaturen, reaktionstiden og piperidinkoncentrationen justeres.
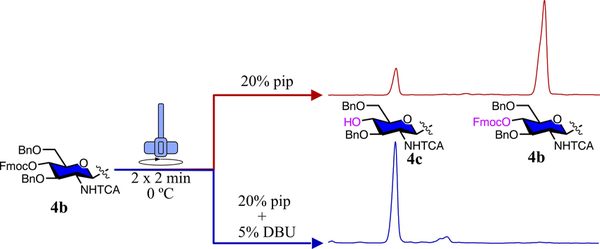
Efter afbeskyttelsestrinnet fjernes Fmoc-gruppen selektivt fra N-terminalen af den voksende peptidkæde, hvilket efterlader sidekædebeskyttelsesgrupperne og peptidrygraden intakte. Det afbeskyttede sted kan derefter anvendes til det næste trin i peptidforlængelse eller yderligere manipulationer som en del af synteseprocessen.
Det er værd at bemærke, at betingelserne for Fmoc-afbeskyttelse kan variere afhængigt af den specifikke peptidsekvens, arten af den Fmoc-beskyttede aminosyre og andre faktorer i synteseprotokollen. Derfor er det vigtigt at henvise til etablerede metoder og litteratur, der er specifik for den peptidsyntese, der udføres.
Hvis du vil vide mere om dette produkt, er du velkommen til at kontakte Xi'an Sonwu.
E-mail:sales@sonwu.com





